Lưu huỳnh (ký hiệu S) là nguyên tố hóa học được nhắc đến khá nhiều trong sách giáo khoa các cấp. Vậy S hóa trị mấy? Lưu huỳnh có ứng dụng như thế nào với cuộc sống hiện nay? Các bạn hãy cùng VietChem khám phá trong bài viết bên dưới.
1. Lưu huỳnh là gì?
Lưu huỳnh là nguyên tố hóa học được ký hiệu là S. Chúng có nhiều tên gọi khác nhau như: Diêm sinh, lưu hoàng, sulfur…
Trong bảng tuần hoàn các nguyên tố hóa học, lưu huỳnh có số nguyên tử là 16. Tức là có 16 hạt proton trong hạt nhân của mỗi nguyên tử. Lưu huỳnh thuộc chu kỳ 3 và nằm trong danh mục các phi kim phổ biến.
Lưu huỳnh có vai trò quan trọng với sự sống của sinh vật, con người. Lưu huỳnh là một phần trong quá trình tạo nên cấu trúc cho ARN, ADN và acid nucleic.

Lưu huỳnh có nhiều tên gọi khác như lưu hoàng, diêm sinh
2. S hóa trị mấy?
Hóa trị của lưu huỳnh khá đa dạng. Bao gồm: Hóa trị 2, hóa trị 4 và hóa trị 6 tùy từng trường hợp liên kết với chất nào trong phân tử.
Ví dụ: Lưu huỳnh có hóa trị 2 trong hợp chất: H2S
Lưu huỳnh có hóa trị 4 trong hợp chất: SO2
Lưu huỳnh có hóa trị 6 trong hợp chất: SO3

Lưu huỳnh có hóa trị 2, 4 và 6
3. Tính chất vật lý của lưu huỳnh
Lưu huỳnh là nguyên tố hóa học có nhiều trong tự nhiên. Khi đó, chúng tồn tại ở dạng đơn chất hoặc khoáng chất. Lưu huỳnh tìm thấy trong các khoáng chất sunfat và sunfua.
Lưu huỳnh có 2 dạng tồn tại là lưu huỳnh đơn tà và lưu huỳnh tà phương. Ở điều kiện nhiệt độ khác nhau, chúng sẽ có những tính chất đặc trưng tương ứng. Cụ thể:
- Nhiệt độ dưới 1130C: Lưu huỳnh là chất rắn có màu vàng đặc trưng.
- Nhiệt độ 1190C: Lưu huỳnh bị nóng chảy thành chất lỏng có màu vàng.
- Nhiệt độ 1870C: Lưu huỳnh chuyển sang dạng lỏng dẻo màu nâu đỏ.
- Nhiệt độ 4450C: Đây là nhiệt độ sôi của lưu huỳnh, các cấu trúc của S bị phá vỡ và dễ bay hơi.
- Nhiệt độ 17000C: Hơi lưu huỳnh chính là nguyên tử S.
Trong cơ thể con người, S hóa trị mấy không quan trọng bởi chúng là thành phần thiết yếu. S được tìm thấy trong 2 loại axit amin góp phần duy trì sự sống.
Nhiệt độ dưới 113 độ C, lưu huỳnh là chất rắn có màu vàng
4. Tính chất hóa học của lưu huỳnh
Lưu huỳnh có nhiều hóa trị cùng khả năng hoạt động tốt nên sở hữu nhiều tính chất hóa học đặc trưng. Bao gồm:
4.1. Tác dụng với kim loại
Ở điều kiện nhiệt độ, lưu huỳnh có thể tác dụng với kim loại để tạo ra những sản phẩm có số oxi hóa thấp hơn kim loại. Ví dụ:
- Zn + S → ZnS
- Fe + S → FeS
Ngoài ra, phản ứng của lưu huỳnh với kim loại còn tạo ra một số muối đặc trưng. Các muối sunfua nổi bật như: CdS màu vàng, MnS màu hồng, các muối PbS, CuS, Ag2S… có màu đen.
4.2. Lưu huỳnh tác dụng với hidro
Dựa vào kiến thức S hóa trị mấy sẽ nắm được tính chất hóa học của lưu huỳnh. Với hóa trị đa dạng 2, 4, 6, lưu huỳnh có tính oxi hóa mạnh với hidro ở nhiệt độ 3500C. Phương trình phản ứng như sau: H2 + S → H2S.
Một số phương trình phản ứng khi cho lưu huỳnh tác dụng với các hợp chất có tính oxi hóa mạnh như sau:
- S + 4HNO3 đặc → 2H2O + 4NO2 + SO2
- S + 2H2SO4 đặc → 3SO2 + 2H2O
4.3. Lưu huỳnh tác dụng với phi kim và hợp chất có tính oxi hóa mạnh
Lưu huỳnh có thể tác dụng với 1 số hợp chất có tính oxi hóa hoặc phi kim do có tính khử. Trong đó, phản ứng điển hình nhất là tác dụng với oxi:
- S + O2 → SO2
Một số phương trình phản ứng khi cho lưu huỳnh tác dụng với các hợp chất có tính oxi hóa mạnh như sau:
- S + 4HNO3 đặc → 2H2O + 4NO2 + SO2
- S + 2H2SO4 đặc → 3SO2 + 2H2O
5. Cách sản xuất lưu huỳnh
Lưu huỳnh có nhiều cách sản xuất trong công nghiệp hoặc điều chế trong phòng thí nghiệm. Cụ thể:
5.1. Điều chế lưu huỳnh trong phòng thí nghiệm
Điều chế lưu huỳnh bằng cách đốt nóng H2S hoặc khử khí lưu huỳnh đioxit.
- Đốt H2S (hydro sulfide) trong điều kiện không có không khí.
Phương trình phản ứng: 2H2S + O2 → 2S 2H2O
- Khử lưu huỳnh đioxit kèm theo chất xúc tác hydro sulfide.
Phương trình phản ứng: 2H2S + SO2 → 3S + 2H2O
5.2. Khai thác lưu huỳnh trong tự nhiên
Trong tự nhiên dưới lòng đất, lưu huỳnh có thể được khai thác số lượng lớn. Sử dụng ống nén nước ở 1700C để thu được lưu huỳnh nóng chảy. Sau đó S nóng chảy sẽ chảy lên mặt đất và khai thác bằng hệ thống máy móc chuyên dụng.
Lưu huỳnh thu được ở dạng lỏng sau khi nguôi. Cuối cùng là chuyển thành dạng bột để sử dụng.
6. Ứng dụng của lưu huỳnh
Lưu huỳnh được ứng dụng khá phổ biến trong y học và công nghiệp. Cụ thể:
- Ứng dụng của lưu huỳnh trong y học: Sử dụng lưu huỳnh để điều chế một số loại thuốc chữa bệnh như: thuốc nhuận tràng, thuốc có khả năng kháng khuẩn, kháng viêm để chữa bệnh rối loạn ngoài da.
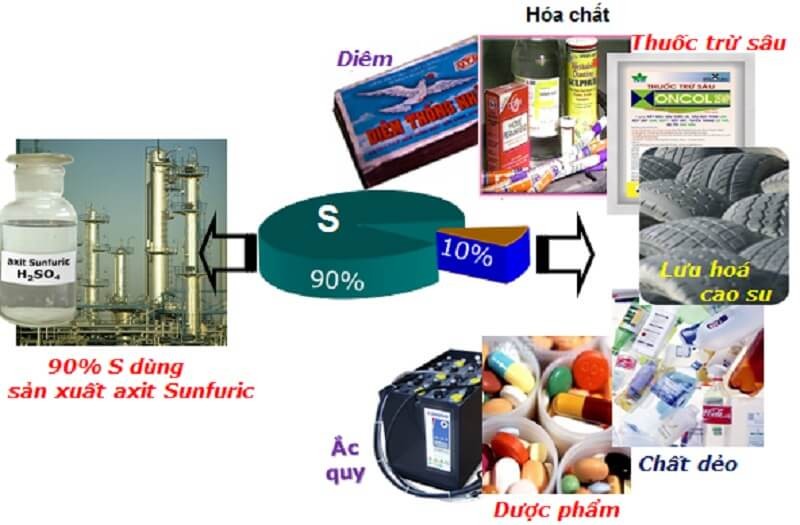
- Ứng dụng của lưu huỳnh trong công nghiệp: Dùng để sản xuất thuốc súng, diêm, bột giặt, thuốc nhuộm. Lưu huỳnh cũng được sử dụng để lưu hóa cao su và sản xuất acid sulfuric H2SO4.
- Ứng dụng của lưu huỳnh trong nông nghiệp: Lưu huỳnh là nguyên liệu trong sản xuất thuốc diệt nấm, thuốc trừ sâu, phân bón…
Lưu huỳnh có nhiều ứng dụng trong cuộc sống
S hóa trị mấy đã được chia sẻ cụ thể trong bài viết trên. Hy vọng những chia sẻ sẽ giúp các bạn hiểu rõ hơn về nguyên tố hóa học quan trọng và cần thiết này. Nếu muốn tìm hiểu về S và các nguyên tố hóa học khác, các bạn hãy liên hệ với VietChem theo số hotline của chúng tôi để được giải đáp.