Oxit: Thuật ngữ quen thuộc trong hóa học

Oxit là gì? Chắc hẳn ai trong chúng ta cũng ít nhiều đã nghe hoặc nhìn thấy thuật ngữ này trong các bài tập hóa học hoặc trong cuộc sống hàng ngày. Vậy oxi là gì? Phân loại oxit và các tính chất hóa học của oxit như thế nào?
Cùng máy lọc nước Karofi tìm hiểu chi tiết về các thông tin liên quan đến thuật ngữ oxit trong bài viết dưới đây. Theo dõi ngay!
Oxit là gì?
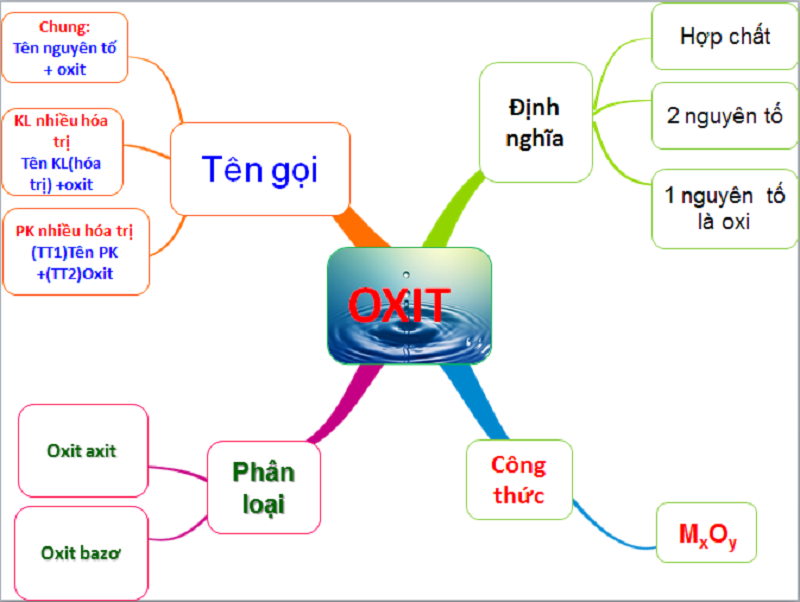
Oxit là tập hợp các hợp chất gồm 2 nguyên tử hóa học, trong đó có một nguyên tử oxy. Ví dụ: N2O5, CaO, CuO, Fe2O3, SO3, SO2, P2O5, CO2,…
Công thức hóa học của các loại oxit được biểu diễn dưới dạng MxOy.
Sau đây là cách đọc tên đối với các loại oxit cụ thể:
-
Đối với kim loại, phi kim có 1 hóa trị = tên nguyên tố + oxit. Ví dụ:
- NO: Nitơ oxit
- CaO: Canxi oxit
- Al2O3: Nhôm oxit
- Na2O: Natri oxit
- K2O: Kali oxit
-
Đối với kim loại có nhiều hóa trị = tên kim loại + (hóa trị kim loại) + oxit. Ví dụ:
- FeO: Sắt (II) oxit
- Fe2O3: Sắt (III) oxit
- CuO: Đồng (II) oxit
-
Đối với phi kim có nhiều hóa trị = (tiền tố của nguyên tử phi kim) + tên phi kim + (tiền tố của nguyên tử oxit) + oxit. Trong đó:
- Tiền tố Mono là 1
- Tiền tố Đi là 2
- Tiền tố Tri là 3
- Tiền tố Tetra là 4
- Tiền tố Penta là 5
- Tiền tố Hexa là 6
- Tiền tố Hepta là 7
- Tiền tố Octa là 8
- Tiền tố Nona là 9
- Tiền tố Deca là 10
Ví dụ:
- CO: Cacbon mono oxit (tên gọi đơn giản là Cacbon oxit)
- SO2: Lưu huỳnh đioxit
- CO2: Cacbon đioxit (tên gọi đơn giản là Cacbonic)
- SO3: Lưu huỳnh trioxit (tên gọi đơn giản là Sunfurơ)
- P2O5: Điphotpho pentaoxit.
Phân loại oxit
Oxit được chia thành 2 loại chính là oxit axit và oxit bazơ, cụ thể:
-
Oxit axit: Đây thường là các oxit của phi kim. Khi cho oxit axit tác dụng với nước, sẽ tạo ra axit tương ứng. Ví dụ:
- CO2 + H2O → H2CO3
- SO2 + H2O → H2SO4
- SO3 + H2O → H2SO3
- P2O5 + H2O → H3PO4
-
Oxit bazơ: Đây là các oxit của kim loại. Khi cho oxit bazơ tác dụng với nước, sẽ thu được bazo tương ứng. Ví dụ:
- CaO + H2O → Ca(OH)2
- CuO + H2O → Cu(OH)2
- Fe2O3 + H2O → Fe(OH)3
- Na2O + H2O → NaOH
-
Oxit lưỡng tính: Đây là các oxit có khả năng tác dụng với cả axit và bazơ, sau đó tạo ra muối và nước. Ví dụ: ZnO và Al2O3.
- ZnO + 2HCl → ZnCl2 + H2O
- ZnO + 2NaOH → Na2ZnO2 + H2O
-
Oxit trung tính: Đây là loại oxit không có phản ứng hòa tan trong nước, không tác dụng với cả axit và bazơ như CO và NO.
Ngoài các loại oxit trên, còn có một loại oxit khác được gọi là oxit hỗn tạp. Loại oxit này không phổ biến và thường được coi là một loại oxit hoặc muối.
Ví dụ:
- Fe3O4 = Fe(FeO2)2 tên gọi là Sắt (II) ferit
- Pb2O3 = PbPbO3 tên gọi là Chì (II) metaplombat
Tính chất hóa học của Oxit
Mỗi loại oxit có các tính chất hóa học riêng, cụ thể:
-
Tính chất của oxit axit:
- Tác dụng với nước: Khi oxi axit tác dụng với nước, sẽ tạo ra axit tương ứng. Ví dụ:
- SO2 + H2O → H2SO4
- Tác dụng với bazo: Oxit axit tác dụng với các bazo kiềm là NaOH, Ca(OH)2, KOH, Ba(OH)2.
- CO2 + KOH → K2CO3 + H2O
- SO2 + Ba(OH)2 → BaSO3 + H2O
- Tác dụng với oxit bazơ: Oxit axit tác dụng với oxit bazơ tạo ra muối tương ứng.
- Na2O + CO2 → NaCO3
- CaO + CO2 → CaCO3
- Tác dụng với nước: Khi oxi axit tác dụng với nước, sẽ tạo ra axit tương ứng. Ví dụ:
-
Tính chất của oxit bazơ:
- Tác dụng với nước: Chỉ có các bazo kiềm là Na2O, CaO, K2O và BaO tác dụng với nước. Sau phản ứng, thu được dung dịch kiềm.
- BaO + H2O → Ba(OH)2
- Na2O + H2O → NaOH
- Tác dụng với axit: Oxit bazơ tác dụng với axit tạo muối tương ứng và nước.
- CaO + 2HCl → CaCl2 + H2O
- Na2O + H2SO4 → Na2SO4 + H2O
- Tác dụng với oxit axit: Oxit bazơ tác dụng với oxit axit tạo muối.
- Na2O + CO2 → NaCO3
- CaO + CO2 → CaCO3
- Tác dụng với nước: Chỉ có các bazo kiềm là Na2O, CaO, K2O và BaO tác dụng với nước. Sau phản ứng, thu được dung dịch kiềm.
Như vậy, thông qua bài viết này, Karofi Việt Nam đã giải đáp cho bạn đọc về oxit là gì, phân loại và tính chất hóa học của oxit. Hy vọng bạn đã tìm thấy những kiến thức hữu ích để áp dụng trong quá trình học tập và làm việc của mình!
►► Xem thêm: